2026年1月号
挑戦する研究者たち
最新のICTをいち早く医療へ応用、新たなアプローチで心疾患など病気の早期発見に挑む

昨今、1つの専門、学問だけでは課題解決は難しく、複数の領域にまたがった横断的な研究が重要視されるようになってきました。医療の分野も例外ではなく、情報通信や新素材をはじめとする他分野とのコラボレーションが欠かせなくなっています。そのような中、NTT物性科学基礎研究所の塚田信吾フェローは、いち早く医療領域へICTを取り入れた、医療・ICT学際領域の先駆者です。今回、ヒューマン・メタバースの実現をめざした国際的プロジェクトへの参加やテンソル心電図の詳細な状況、そして医師でありながらNTTで基礎研究を志向する思いについて伺いました。
塚田信吾
フェロー
NTT物性科学基礎研究所
ヒューマン・メタバースで全身機能を再現、病気の研究や治療に役立てる
大阪大学WPI-PRIMeでの共同研究についてお聞かせください。
ここ数年でChatGPTを代表するLLM(大規模言語モデル)などAI(人工知能)により研究を取り巻く環境が劇的に変化してきたと感じています。また、これらの与える影響は情報通信にとどまらずさまざまな領域に及んでおり、私が専門とする医療の領域にも大きなインパクトを与えています。
臨床の現場でも検査値や画像をはじめさまざまなデータのデジタル化が進む中、AIの利用も活発になってきました。同時に、iPS細胞の研究に代表される遺伝子・分子・細胞の研究も急速に進歩しており、その中にAIを取り入れる動きも活発化しています。こうした変化は私たちが想定していた以上に加速している実感があります。私たちNTT研究所はこれからの時代を見据え、大学医学部や大学病院とより深く連携しながら、基礎研究を進めていく必要があると考えています。
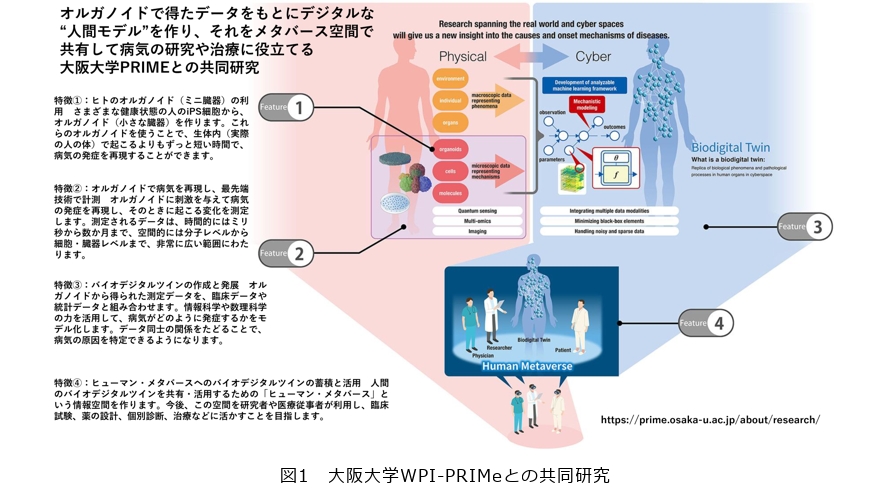
一方で、現状の医学の現場では遺伝子や細胞レベルのデータと、実際の高齢者など成人の病理との間にはまだ大きなギャップがあります。これを埋める基礎研究も加速していく必要があり、それを推進する国際的な拠点として、独立行政法人日本学術振興会(JSPS)支援のもと大阪大学にヒューマン・メタバース疾患研究拠点(WPI-PRIMe)が新たに設立され、私は企画段階からこのプロジェクトにかかわってきました(図1)。
ここでは、ヒトの細胞からiPS細胞をつくり、そこから心臓や肝臓など1ミリ程度の非常に小さな臓器を生成しています。提供者の体内の臓器を傷つけることなく、皮膚や血液から細胞を採取し、試験管中で臓器を作製できる時代になったということです。
もちろん、これには技術的な課題があります。その1つが、現状、胎児から赤ちゃん程の成熟度の組織までしか生成することができず、大人の成熟した組織をつくることはできません。組織の成熟化の過程では血管が重要な役割を果たします。血管により立体的な構造の組織としてある程度の大きさまで成長しないと、十分な機能を発揮することができない場合が多いのですが、現時点では血管をつくることが非常に難しいのです。しかし、この小さな臓器でも遺伝子の変異や、薬剤や環境による異常の再現ができるようになってきました。この新しい技術であるオルガノイドを使って細胞、遺伝子の病気を再現する研究を進めています。
しかし、先ほどからお伝えしているとおり、オルガノイドで再現できるのは、主に幼弱な段階で異常を現す先天性疾患が対象で、より一般的で複雑な成人の病気を再現するまでには至っていません。私たちはそのギャップについてAIやシミュレーションなどを活用し、デジタル空間上に再現する計画に取り組んでいます。ここではiPS細胞などを専門とするバイオの研究者や生命科学情報(バイオインフォマティクス)の研究者、AIなど数理モデルを得意とする研究者など多彩なメンバが集まり、NTT研究所の研究者も多数参加し、多角的に研究を推進しています。また、日本人だけでなく海外の研究者も多数参画し、国際色豊かなチームが構成されています。この異分野の交流により、各臓器をデジタルツイン上に再現し、最終的にはヒューマン・メタバース(アバター)で全身機能を再現していくという、未来志向の研究を実施しています。
情報通信で培った波形解析技術を医学で活かす
現在取り組まれているテンソル心電図について詳しく教えてください。
日本では超高齢化社会となり、心不全の患者が増え、心不全パンデミックともいわれています。よって心疾患を早期に発見し治療する技術の確立は急務といえます。心臓は私の専門領域にもあたり、テンソル心電図という技術を開発しています。これは心電図の波形を数理的に解析することで、今まで見えていなかった初期の病変も可視化できることが分かりつつあり、画期的な解析手法の1つと自負しています。
心電図の技術は100年以上の歴史があり、世界で幅広く利用されているのですが、実は現在の医療水準からすると正常値のばらつきが多く、心電図検査だけで心臓のすべての異常を見つけるのは難しいのです。心臓病の種類にもよりますが、病気がかなり進行した状態でないと診断ができないことが多くあります。
現在、この分野では機械学習による心電図解析も盛んに行われていますが、大量のデータによる事前学習が必要です。しかし、心臓疾患の中には希少疾患もあり、その稀な病気のデータを大量に集めるのは困難です。また、心臓病は発作から心停止までのリードタイムが短く、異常検知から即座に対応、あるいは事前に異常を検知する必要があります。機械学習で高速処理による監視を行うには、相当の処理能力が必要です。さらには、その判定の医学的根拠を説明することが難しいという課題も残されています。
私たちは前述の課題をテンソル心電図のシステムが有効に解決できるのではと考え、研究を進めています。心電図波形の振幅、時間、幅の計測や全体波形の特徴をみることで、正常か異常かを大別する手法は100年以上もの間、基本的に変わることがなく、情報通信や数理解析の専門家からみると、「まだこのような状況にあったのか」といわれてしまう始末でした。私もNTTに入社してから、多くの研究者とさまざまな物理モデルについて話していると、心電図の解析技術の遅れに問題意識を持つようになり、この研究を始めるきっかけにもなっています。
そこで、心電図の波形をガウス関数でモデル化することを試みたのです。ガウス関数を累積分布で表すと、下から上に滑らかに上昇していく独特の形になることに着目し、心臓における電気的興奮の伝わり方を、ガウス関数でモデル化できないかと考えたのです。
心臓では、電気的な興奮が内側から外側へ伝わることから始まる一方で、興奮からの回復は逆に外側から内側へ伝わるという特徴があります。また、心筋は一度興奮するとしばらくその状態を保ち、一定時間が経過してから回復に移るという性質を持っています。この興奮の持続時間は内側と外側で異なり、その差が波形の形状に影響を与えます。
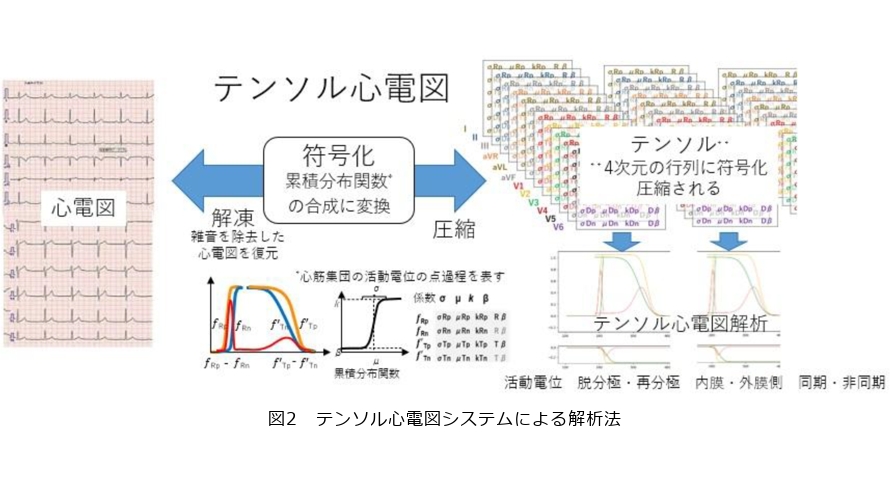
こうした心臓における興奮と回復の2つの電気活動(活動電位)をそれぞれガウス関数で表すモデルを考案しました。心臓の内側と外側の心筋の活動電位の差分が心電図の波形とほぼ一致することは古典的な教科書でうたわれており、心電図の双極子モデルと呼ばれています。実際、私たちのデータにおいて2つの累積分布関数の差分をとると、この波形は実際の心電図波形と一致することが分かり、この解析方法と医学的に確立された理論とが直接結び付けられました。シンプルな形状の心電図であれば、4つだけの累積分布関数の組合せで表現できるようになりました。また実際の臨床でも、10個程度の累積分布関数を組み合わせることで表現できるようになりました(図2)。このアイデアは十分に実用性があり、世界の研究者も未検討であることから、解析モデルとして特許を出願し、各国で成立させています。
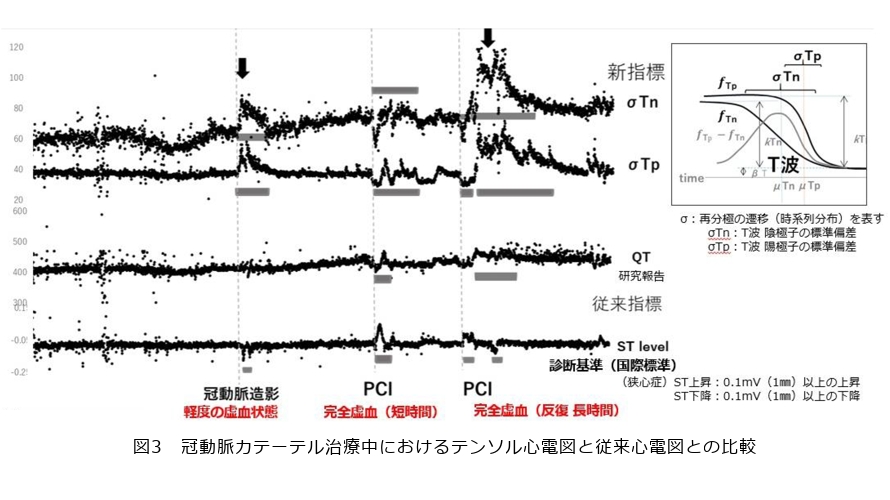
研究を進める中で、この手法が想像以上に大きな効果をもたらすことも最近明らかになってきました。例えば心筋梗塞が発生する際には、心臓への血流が不足し、従来は心電図の評価指標として「ST部分」と呼ばれる波形の基線レベルの上昇や下降が用いられてきました。しかし、このSTの変化が検出されるのは、心臓がかなり強い虚血状態に陥り、血流がほとんど途絶えるような段階になってからです。
一方、今回の新しい指標では、波形の平均値や分散といった特徴量を高精度にパラメータ化することができるため、時間軸上の微小な変化をより鋭敏にとらえることが可能となり、心臓の血流状態の変化を早期に検出できる可能性が示されました(図3)。
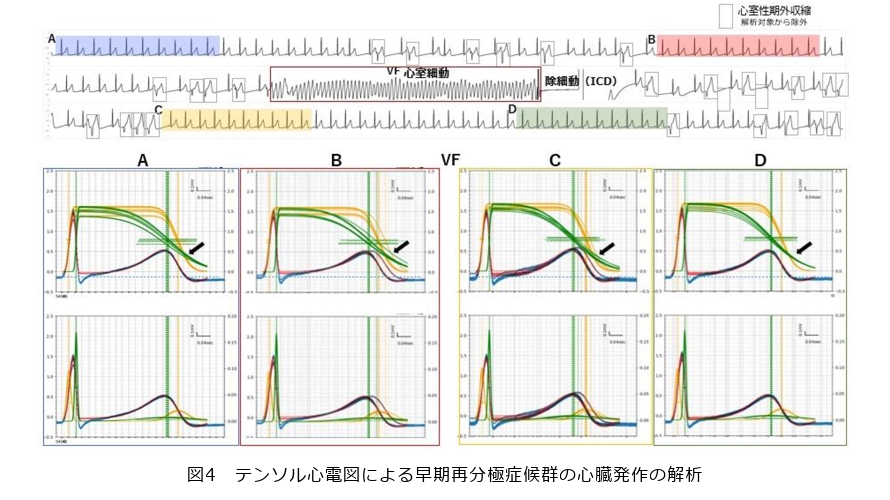
突然死の原因となる心室細動は、心臓の筋肉が痙攣するように不規則に収縮する状態を示しますが、その発作の前段階には、一見すると正常に見える「不安定な時期」が存在します。通常の心電図では、この時期の異常を視覚的に判断することはほとんどできません。ところが、心電図波形をガウス関数やその累積分布関数に基づいて解析してみると、心筋の内側と外側とで興奮から回復する順序が逆転していることが確認されました。さらに、発作直前になると、この逆転の仕方や興奮からの回復分布が大きく乱れることも明らかになりました(図4)。この変化を精度良く検出できるようになれば、心室細動が起こる前にその兆候をとらえ、適切な処置を行うことが可能になると考えられます。
目下の課題としては、この研究が医学的ではなく情報通信的な発想に基づいているため、医学関係の研究者に理解していただくのが難しく、デジタルヘルスの専門誌に論文を投稿したところ、レビュワーが見つからないという理由で1年ほど受理されませんでした。そういった意味でもパイオニアとしての苦労を実感しています。一方で、AIや情報通信の分野の専門家に説明すると、「これは通常のアプローチですね」とご理解いただけることが多く、その点では少し安心しています。
医学の教科書には心筋梗塞時の活動電位について掲載されてはいるものの、これは過去、動物実験などで傍証を得た結果で、人間の心臓で確認されたデータではありません。私たちのシステムで患者の心電図を解析すると、この教科書に掲載されているとおりのパターンになっていることが分かっていますので、いずれ医学界でも広く認めていただけるのではないかと、今後もコツコツと実験を積み重ね、発表していきたいと思います。
細胞、遺伝子レベルでのミクロな生体観測に向け、hitoe®などオリジナル技術を発展
今後の研究の展望についてお聞かせください。
現在、私たちが計測している生体情報は心電図の波形データのようなマクロ量、すなわち心臓を構成する1つひとつの細胞のバルクとしての情報になりますが、これを細胞や分子あるいは遺伝子スケールのミクロレベルに観測することで、より細胞学的、遺伝子学的な見地から病気や心身の不調を解明することができると考えられます。
最近、チップレベルで小さな臓器などの組織を作製し、創薬の実験などへ適用することができるようになりました。そのチップの中でオルガノイドを育てることが最近のブームになっており、1つのデバイスとして私たちが心電図の検査用衣服として東レと共同開発したhitoe®の技術をマイクロ化することで、iPS細胞用の電極を作成できるようになりました。これには微細加工の技術にも並行して取り組む必要があり、基礎研究からiPS細胞を扱っている研究者たちともコラボレーションしています。
このようなミクロレベルでの心臓のモデル化やデジタルツイン化は、世界中の研究者も注目し、皆が競って取り組んでいるところですから、研究として突出するには差別化した技術を持つ必要があります。私たちの場合はテンソル心電図と、hitoe®という生体適合性の高い電極、この2つの独自技術を所有しているため、これらを分子・遺伝子のミクロと心電図のマクロに適用し、スケールの異なる異常を結び付け、オリジナリティの高いデータを取得することをめざしています。
さらにミクロなレベルで得られたマルチモーダル、マルチスケールの情報をマクロレベルに生成加工したり、将来的には日本中で計測されている心電図のビッグデータの解析に適応していけるようにコツコツと取り組んでいきたいと考えています。
医療とICTは将来深くかかわるというビジョンを描いて
医師でありながらICT企業であるNTTに入社されたきっかけや思いについてお聞かせください。
私はもともと臨床外科医師でしたが、後に神経の再生にかかわる基礎研究者へとシフトしました。それをきっかけに米国カリフォルニア大学サンディエゴ校(UCSD)へ留学する機会を得て、そこでは脊髄損傷の遺伝的再生医療の研究をしていました。
当時はiPS細胞がまだ開発される以前で、ES細胞を神経に分化させ、これを移植する研究に取り組んでいました。UCSDは産学連携がとても盛んで、良い技術や特許があると、速やかに社会実装していくスピード感に溢れた行動がみられ、大変驚きました。
大学の先生たちも社会実装を念頭に置きながら活発に活動されており、その姿を目の当たりにすると、日本へ帰国後も大学で働いていくことが自分にとって果たして良いことなのかと疑問が生まれてきました。
実際、帰国し一度大学に戻ったのですが、やはり前述の留学時の思いも強く、先端的な基礎研究が盛んで、光通信などでは社会実装にも積極的に取り組んでいるNTTの姿勢に感銘を受け、勇気をもって入社を決意しました。
NTT物性科学基礎研究所(物性研)に入所した当初は、脳と直接通信する、ブレインマシンインタフェースの研究に取り組みましたが、その理由は、脊髄損傷の治療の1つの戦略として有効ではないかと考えていたためです。この分野では、米国にイーロン・マスクらが共同設立したニューラリンクがありますが、当時日本では、物性研しか選択肢はなかったのです。
私は、ブレインマシンインタフェースの研究だけをしたかったわけではなく、幅広く日本の先端技術を医療の現場に応用していく研究がしたかったのです。例えば最先端の素材やデバイス、そして近年急速に発展してきたデジタル分野、すなわち情報通信やAIの技術などもその対象です。医学でもこれらの先端技術により、古典的なシミュレーションや診断法が突然進化するときが来るのではないかと考えていたからです。
留学中にシリコンバレーやサンディエゴで知り合った技術者には、京セラやソニーをはじめ、日本のさまざまな企業から派遣された方もおり、特にサンディエゴにはクアルコムの本拠もあるため通信を専門とする留学生が多数いました。その交流の中で情報通信の面白さを実感し、帰国後にNTTにご縁をいただき、今回お話ししたテンソル心電図というアイデアに結び付けたり、hitoe®を開発したりと、さまざまな興味深いプロジェクトにかかわることができました。
大局的にビジョンを描き、自ら動いて仲間をつくり、自ら取得したデータを重視しよう
後進に向けてメッセージをお願いします。
基礎研究の分野も国際競争が激しさを増し、LLMやAIの研究も大規模化してきました。そのような中で一研究者としていったい何ができるのだろうかと自問自答する機会が多いと思います。
実際に私も若いころから今に至るまでずっと悩んできているわけですが、情報も爆発的に増えているなど激しい変化が起きている時代でどう立ち回っていくべきかという問いに対して、私自身の考えを述べたいと思います。
1つは、何となくでも結構ですから、自分の取り組んでいる研究は「将来どうなっていくのか」という大局的な予想やビジョンを持つことだと思います。
私が米国に留学したとき、多くの人との出会いの中で、医学やバイオの領域は近い将来、情報通信の領域と深くかかわり、AIなどを活用する時代になっていくのではと、何となく想像するようになりました。ですから、皆さんの各専門領域においても、時代の流れを読み取り、将来の大局的な予想、ビジョンを立ててみてはいかがでしょうか。
2番目は、その予測にのっとって、実際に行動を起こすことです。例えば、今回の大阪大学のPRIMeのプロジェクトに関しても、先方からの声掛けに私が反応したところからスタートしています。つまり、社内外問わず仲間をつくって行動することは大切だと思っており、若い方こそ、精力的に行動を起こしていっていただけたらと思います。
3番目は、研究は国際競争の中で業績や結果を出さなければいけない世界であるため、厳しい評価を受ける場面もあり、ついつい守りの思考に陥ってしまいがちです。しかし、コンセプト創りなど発想は常に自由奔放に、失敗を恐れず攻めの姿勢をとっていただきたいと思います。同時に、求められる業績や結果にもこたえていく、これらをバランスさせて両立していければ良いのではと思います。
最後に、例えば近年、LLMなどの機械学習に絡んだ研究が科学雑誌や国際学会などで大きく取り上げられ、その最先端の発表内容や情報量に圧倒されてしまうことがあります。しかし、LLMは私たちに莫大な知識情報を提供しますが、1つひとつの情報や実験データをLLM自身が集めているわけでもなく、試行錯誤しながら研究しているわけでもありません。
あくまで言語化され、公開されている情報から大量に学んでいるにすぎません。それに対して、私たち研究者の強みは自分の手で実験し、あるいは自分の足で丹念に拾い集め手に入れた実測データ、すなわち記号化、言語化される前のデータを体験とセットで持っていることなのです。
私はここに至るまで、紆余曲折あり悩んできたこともたくさんありましたが、最後に自分を救ってくれたのは自分が直接取得したデータ、実験結果だと信じています。自分のデータを丹念に見ていくと、そこには真理が示されていることが多々ありました。自分のデータは自分の道標になっていると感じており、これまで気付かなかったことを教えてくれているのですね。AIはあくまで補助手段として使いこなし、地道にコツコツと汗をかきながら自らデータの取得や解析を積み重ねていくことに重きを置いていただけたらと思います。




